北醫揭露自家卵巢癌數位病理AI進展,目前模型可辨識肉眼難以分辨的兩大癌症亞型,也能進一步分辨亞型中的腫瘤細節。
攝影/王若樸
臺北醫學大學病理學科教授陳志榮昨(7日)揭露北醫卵巢癌病理切片AI進展,目前已能準確識別、定位兩種肉眼難以辨識的卵巢癌腫瘤組織,也就是漿液性癌和子宮內膜樣,可幫助醫生加速判讀和制定醫療策略。這套AI模型的敏感度和特異性分別達0.93和0.96以上,未來,北醫打算擴大醫院訓練資料的採樣範圍,以更多元的訓練和驗證資料,來優化模型。
卵巢癌發生率節節上升,醫生得格外小心判斷高相似度的兩種亞型
北醫3年前開始接觸數位病理AI,聚焦領域也從胸腔腫瘤轉移至近來的卵巢癌。卵巢癌號稱女性的沈默殺手,衛福部統計,臺灣卵巢癌發生率占女性十大癌症的第七位,近年更節節上升。陳志榮指出,常見的卵巢癌可分為四種亞型,包括漿液性癌(Serous Carcinoma)、子宮內膜樣癌(Endometrioid Carcinoma)、亮細胞癌(Clear Cell Carcinoma)、黏液性癌(Mucinous Carcinoma)。
為辨識卵巢癌類型,醫生得先進行病理切片,再透過顯微鏡或電腦來觀察玻片上的細胞組織型態。陳志榮指出,亮細胞癌和黏液性癌的病理組織型態特殊、容易診斷,但是,漿液性癌和子宮內膜樣癌就沒那麼簡單了。
它們的腫瘤組織結構相似,細胞型態也可能類似,而且,就算透過免疫組織化學染色的蛋白質標記表現,也不具完全的決定性。所以,病理醫生在診斷漿液性癌和子宮內膜癌時,「就得格外小心;」特別是遇到分化不良(高惡性度)的漿液性癌和子宮內膜樣癌,病理醫生難以從形態學和免疫組織化學染色找到足夠證據,還得請教婦癌病理醫生。
這麼小心是因為,這兩種亞型基因型態、臨床表現不同,相對應的治療策略和病人預後也會有所不同。
收集北醫卵巢癌病理切片打造AI,AUC最高達0.994
因此,陳志榮想建立AI辨識模型,來判別這兩種亞型。於是,他與團隊收集了北醫附醫病理科的卵巢癌病例,將病例玻片掃描、數位化後,再從中挑選漿液性癌和子宮內膜樣癌案例,「總共200張片子。」
接著,他們用其中的180張來訓練模型,以另外20張來測試、驗證。過程中,他們請5位病理醫生標註200張病理切片,包括良性腫瘤、漿液性腫瘤和子宮內膜樣腫瘤,並將影像切割為471um x 471um大小,來訓練模型。之後,模型會根據這些影像,來標示三種腫瘤區域和發生機率。
再來,團隊從幾個訓練模型中,挑出表現最好的一個,來進行驗證。陳志榮指出,雖然只利用180張片子來訓練,但「AI模型已有不錯的表現。」因為,模型對漿液性癌和子宮內膜樣癌的敏感度,分別達到0.995和0.933,其特異性更分別達到0.997和0.966。
而且,就分類效能指標AUC值來說,模型良性腫瘤的AUC值已達最高值1.000,對漿液性癌的AUC值則是0.991,對子宮內膜樣癌則達0.994。
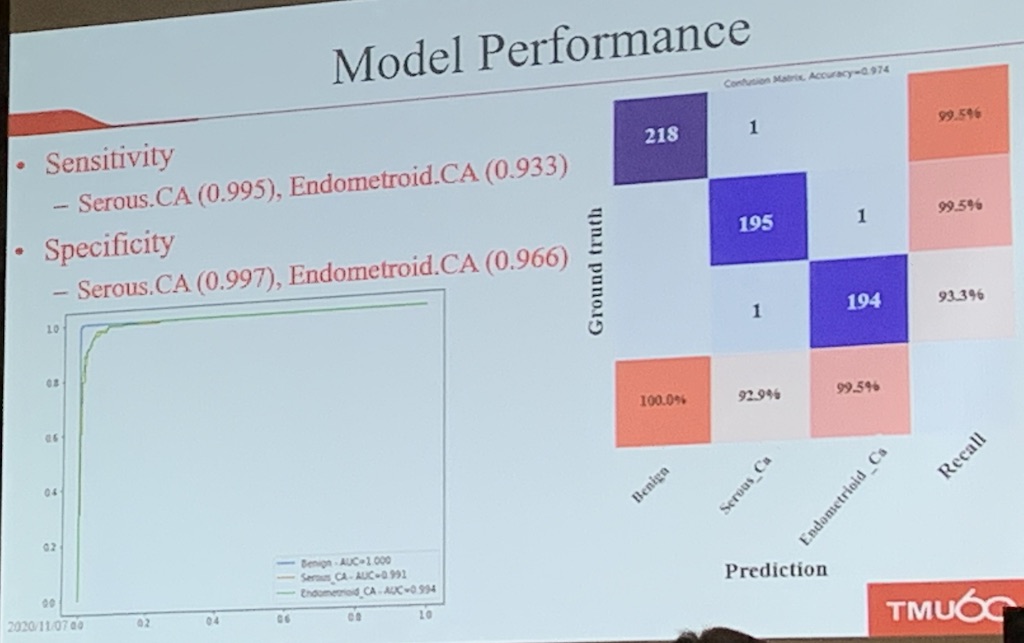
不過,陳志榮指出,模型還是有預測不佳的狀況,比如將子宮內膜樣癌,判斷為漿液性癌。

再接再厲,要讓模型具備更細緻的判斷能力
不只要會辨識兩種卵巢癌亞型,陳志榮還進一步,想讓模型具備更細緻的腫瘤結構判斷能力,也就是說,模型還要會分辨兩種亞型,是否為實質固態瘤或非實質固態瘤(Solid and non-solid)。
他同樣以200張數位病理切片作為資料集,只是在標註上,多了漿液性癌實質固態瘤與非實質固態瘤,以及子宮內膜樣癌(非)實質固態瘤。經測試,模型準確率為0.888,良性腫瘤AUC值依然為1.000,而漿液性癌-實質固態瘤的AUC值為0.989,非實質固態瘤則是0.970;子宮內膜樣癌-實質固態瘤的AUC值是0.979,非實質固態瘤則是0.936。

他坦言,雖然有些AUC值還可以更好,但模型在預測上也有不錯的表現,比如醫生原本將影像標註為子宮內膜樣癌-實質固態瘤,但模型判斷為漿液性癌-實質固態瘤,團隊與醫生討論後,發現確實應為漿液性癌-實質固態瘤,顯示「模型可正確分類。」

未來要擴大資料多元性,還得思考如何與臨床結合
「由此可見,在樣本數不多的情況下,還是能訓練出可辨識腫瘤組織結構的AI,」陳志榮還指出,而且,要讓模型分辨亞型細節,也是可行的。
他也希望,未來能將北醫另外兩家體系醫院納入訓練作業,來增加訓練和驗證資料的多元性;同時也想再賦予模型判斷基因型態的能力。文◎王若樸
熱門新聞
2026-03-02
2026-03-02
2026-03-02
2026-03-02
2026-03-02
2026-02-26
2026-03-02